Per i batteri carnivori il dolore lancinante che provi è una grande opportunità
Lo Streptococcus pyogenes, conosciuto come batterio carnivoro o mangiacarne, quando infetta il corpo provoca un dolore lancinante che promuove la sua invasione, poiché mette ko il sistema immunitario
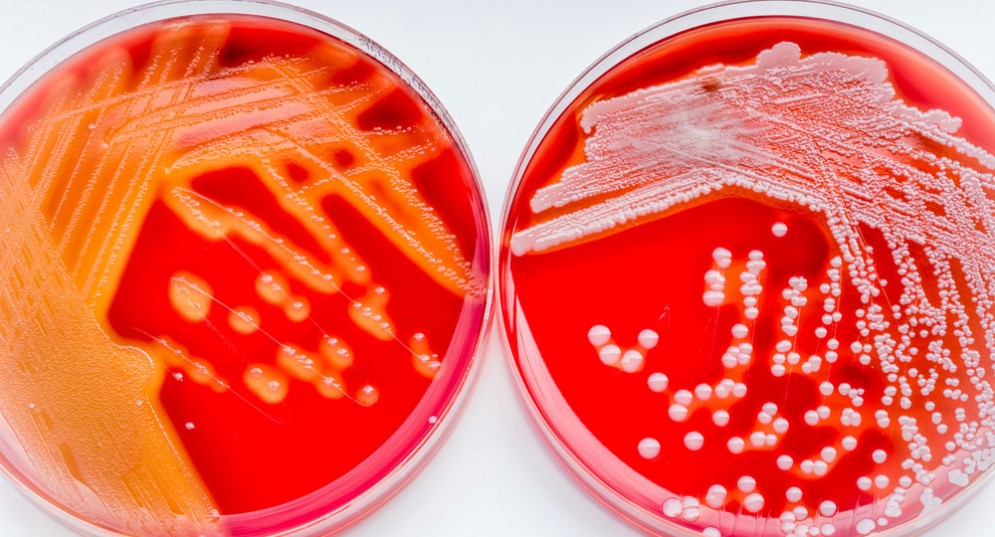
ROMA – Il batterio Streptococcus pyogenes, noto anche come batterio carnivoro o mangiacarne pare sia invero assai intelligente. In particolare, gli scienziati hanno scoperto che riesce a dirottare i recettori del dolore a suo esclusivo beneficio. Questo batterio, che di solito è responsabile del mal di gola è anche causa di una terribile e potenzialmente mortale malattia: la fascite necrotizzante. Durante le fasi iniziali dell’infezione, i batteri emettono una tossina che causa un dolore lancinante. Tuttavia, questo terribile effetto collaterale è molto utile al batterio. Difatti, la sostanza chimica che provoca il dolore intenso ostacola anche il sistema immunitario della persona e crea un ambiente più ospitale affinché il patogeno possa prosperare e riprodursi.
Guerra di intelligenze
Se dunque il batterio Streptococcus pyogenes è intelligente, l’uomo non vuole essere da meno. E in un nuovo studio, pubblicato sulla rivista Cell, gli scienziati hanno mostrato che le stesse armi chimiche che rendono così potente il batterio carnivoro possono contenere anche i mezzi per sconfiggerlo. Studiando infatti l’arsenale tossico dei batteri, i ricercatori della Harvard Medical School, guidati da Isaac Chiu, professore di microbiologia e immunobiologia, potrebbero aver trovato il modo per trasformare il meccanismo a vantaggio del paziente.
La fascite necrotizzante può avere più cause
A provocare la fascite necrotizzante non è solo il batterio Streptococcus pyogenes, ma anche altri come Clostridium, Staphylococcus aureus ed Escherichia coli. Tuttavia, S. pyogenes che è uno streptococco di gruppo A, è quello più comune, sottolineano gli scienziati. Affinché il corpo di una persona possa essere infettato, il batterio necessita che vi sia una ferita o una lacerazione (anche minima) della pelle. Una volta fatto il suo ingresso nell’organismo, il batterio mette in atto la sua terribile strategia per diffondersi. La fascite necrotizzante è così chiamata perché attacca la fascia, ossia il tessuto connettivo che circonda i nervi, i muscoli, i vasi sanguigni e il grasso. È caratterizzata dall’esordio fin dal primo stadio di un dolore intenso, che risulta sproporzionato all’infezione. Nelle fasi successive, l’infezione ha un tasso di mortalità del 32%, riporta lo studio.
La tossina
Nei test condotti sui topi in laboratorio, i ricercatori hanno scoperto che il batterio carnivoro produce una tossina chiamata streptolysin S (SLS). Questa sostanza attiva determinati neuroni correlati al dolore per innescare un dolore lancinante. Questa stessa tossina ha spinto gli stessi neuroni a emettere un peptide che ha interrotto la comunicazione con il sistema immunitario, in modo che il batterio non sia attaccato dalle difese dell’organismo ospite – come di norma avviene. In questo modo, S. pyogenes può liberamente moltiplicarsi e diffondersi distruggendo e divorando la carne di chi è stato infettato. Il peptide, scrivono gli autori, ha anche interferito con la normale funzione delle cellule immunitarie che erano riuscite a raggiungere il sito di infezione, impedendo a esse di erogare un enzima che ucciderebbe i batteri invasivi. ««Questo segnale neuronale – spiega il prof. Isaac Chiu – silenzia il sistema di allarme che normalmente chiama i combattenti dell’infezione del corpo per fermare l’infezione».
Sopprimere il dolore
Dopo aver constatato quanto accade dopo l’ingresso nell’organismo del batterio, i ricercatori hanno ipotizzato che se si agiva sul dolore provocato da rilascio del peptide, era possibile bloccare la disattivazione del sistema immunitario o delle difese dell’ospite. In questo modo, per trattare la fescite necrotizzante è necessario interagire con i neuroni, anziché attaccare direttamente il batterio con dei farmaci.
Il ruolo del botulino
Nei test condotti sui topi a cui era stato iniettato il batterio S. pyogenes, i ricercatori hanno poi iniettato la neurotossina botulinica A, una proteina utilizzata per levigare le rughe del viso e curare gli spasmi muscolari. La tossina botulinica agisce bloccando i segnali nervosi. Dopo questa fase, gli autori hanno osservato che nei topi infetti, la tossina botulinica impediva ai batteri di prendere il sopravvento, indipendentemente dal fatto che i topi ricevessero l’agente bloccante prima o dopo la loro esposizione a S. pyogenes. In un altro esperimento, il team di ricerca ha introdotto un altro composto che ha bloccato il rilascio del neurotrasmettitore e ha messo in pausa il sistema immunitario dell’ospite, impedendo anche che i batteri non venissero rilevati dal sistema stesso.
«I nostri risultati – conclude il prof. Chiu – forniscono un esempio lampante di quanto strettamente intrecciati siano i sistemi nervoso e immunitario e quanto complessa sia la loro interazione nel contesto dell’infezione. Il nostro studio sottolinea anche il potenziale terapeutico del modulare un sistema per influenzare l’altro come un modo per trattare l’infezione».