CRISPR e modificazione genetica degli embrioni. Un problema etico?
La promessa è quella di debellare tutte le malattie più gravi grazie alla tecnica CRISPR sul DNA. Ma prima bisogna fare i conti con chi ritiene ci sia un problema etico
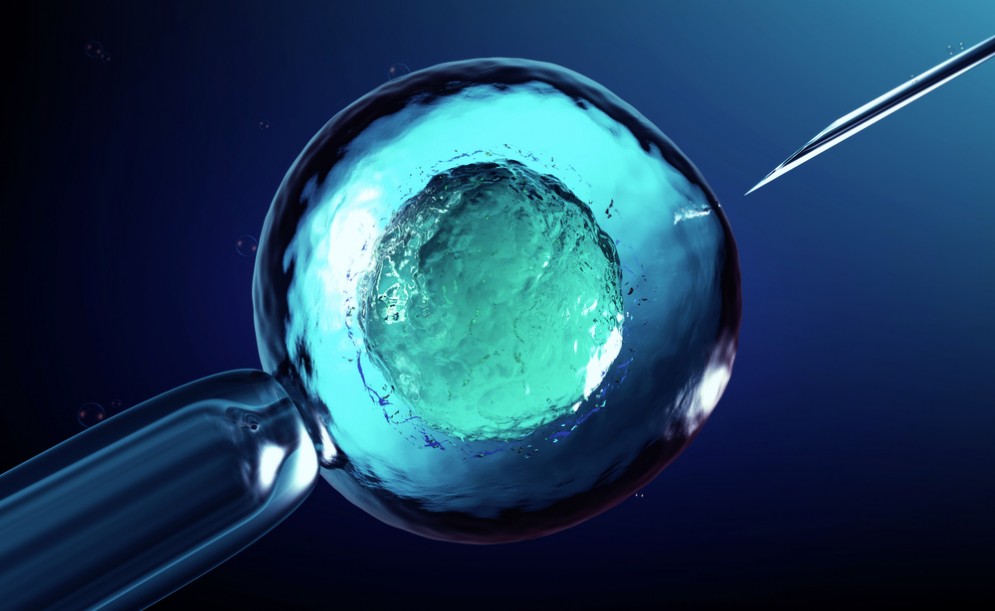
Embrioni modificati geneticamente con la tecnica Crispr-Cas9: è stata questa una delle notizie più discusse della settimana scorsa. Se da un lato il progresso scientifico sta facendo passi da gigante, dall’altro c’è chi rema contro. Un bambino ogm non è accettato dalla maggior parte delle persone. Questa è la dura realtà che si scontra ogni giorno con gli scienziati, quelli veri, in grado di interagire con la vita stessa. Gli unici che nelle proprie mani racchiudono il segreto di una lunga vita. Ma cosa hanno fatto, effettivamente, i ricercatori dall'Oregon Health and Science University? C’è lo spiega, in dettaglio, un articolo pubblicato su Nature e riportato su Le Scienze.
Un problema etico?
Dopo la vicenda no-vax arriva un folto gruppo di persone che si dicono contrarie alla modificazione degli embrioni. «Non si può cambiare un bambino geneticamente». Perché? Si chiedono gli scienziati. Ma è la stessa domanda che ci poniamo anche noi. Nel caso in questione i ricercatori hanno corretto un gene responsabile della cardiomiopatia ipertrofica. Si tratta di un problema che colpisce una persona su 500 ed è responsabile di molti casi di morte improvvisa. Forse sarebbe più corretto lasciare il naturale corso della natura? Magari far soffrire bambini e adulti per una vita intera? Possiamo davvero asserire che preferiamo avere un figlio malato costretto a cure continue, solo per un problema etico? Ma poi, ci chiediamo, dove sta l’etica in tutta questa storia. Vogliamo rimanere fermi alla scienza del neolitico e allo stesso tempo trovare l’elisir di lunga vita? Difficilmente accadrà. E dare una mano alla natura – a nostro avviso – non è sinonimo di mancanza di moralità. O, per usare le parole del professor Darren Griffin dell'università del Kent «E' giusto, moralmente, non intervenire quando abbiamo i mezzi per prevenire una malattia mortale?».
L’alterazione genetica
Per capire meglio che non esiste nessun problema etico alla base di tutto, dobbiamo anche entrare nel dettaglio dell’esperimento. Il gene alterato, responsabile della cardiomiopatia ipertrofica, si trova nel cromosoma 11. Tale mutazione genetica è associata alla proteina MYBPC3, diretta responsabile del mantenimento strutturale del muscolo cardiaco, nonché della sua contrazione e rilascio.
L’utilizzo della tecnica Crispr
Durante la fecondazione in vitro, gli scienziati hanno adottato la tecnica Crispr-Cas9 per intervenire sugli spermatozoi che erano portatori del gene malato. In sostanza, tale metodica prevede l’utilizzo di un enzima che funge come una sorta di forbici che tagliano il gene corrotto. Questo viene poi sostituito con uno totalmente funzionante. In questo caso i ricercatori hanno provato sia con un gene artificiale che con uno naturale, prelevato dalla madre. Infatti non tutti e due i genitori presentavano il gene alterato. Chiaramente gli studi sono ancora in fase iniziale e vi sono tassi di insuccesso. Ma i ricercatori puntano ad avere una maggiore stabilità in futuro: attualmente la percentuale di riuscita è del 72% «Ma contiamo di poter arrivare al 90, se non al 100%», ha dichiarato Shoukrat Mitalipov dell'università dell'Oregon.
Come funzione la tecnica Crispr
Il metodo è molto più semplice a dirsi che a farsi. La tecnica Crisp (si legge crisper) per mezzo di un filamento di RNA – pressoché identico - raggiunge il punto esatto in cui vi è il gene alterato. Possono verificarsi dei problemi solo nel caso in cui alcune regioni del genoma possono avere una grande somiglianza con la sequenza di DNA presa di mira dal filamento di RNA. Va da sé che in questo caso si potrebbe dirigere verso il bersaglio sbagliato.
Non è il primo caso
In realtà non si tratta affatto della prima sperimentazione. Già nei due anni precedenti altri due embrioni erano stati sottoposti a una tecnica simile. Ma durante l’esperimento vi erano stati alcuni problemi. Oggi, però, si è arrivati a un puto di svolta. «Noi abbiamo usato una procedura sicura e abbiamo ottenuto un buon grado di efficienza», spiega Juan Carlos Izpisua Belmonte del Salk Institute. È indubbio, quindi, che le potenzialità di Crisp sono davvero incredibili. Forse un giorno potremo vedere debellate tutte le malattie grazie a questa tecnica. Senza vaccini né farmaci. Sempre che società scientifiche come l'American Society of Human Genetics e il Wellcome Trust britannico, la smettano di mettere i bastoni tra le ruote.
Una buona notizia
Nel frattempo, una buona notizia: l’ufficio europeo dei brevetti ha appena pubblicato un brevetto per l’uso di endonucleasi guidate da RNA per l’ingegneria genetica delle Cellule T. Gli endonucleasi sono degli enzimi che rompono i legami fosfodiesterici interni di una molecola di DNA o di RNA. L’azienda che ha registrato il brevetto è Cellectis, una società biofarmaceutica che si occupa di immunoterapia basata su cellule T-CAR. Il dottor André Choulika, amministratore delegato di Cellectis, ha dichiarato che la sua azienda utilizzerà l’endonucleasi guidata da RNA come Cas9 o Cpf1 per l'ingegneria genetica delle cellule T. «Siamo stati i primi ad esplorare il potenziale di CRISPR nei suoi primi giorni in varie applicazioni, tra cui le terapie e questi primi risultati hanno portato alla concessione di questo nuovo brevetto», ha spiega Choulika all’agenzia stampa UPI. Insomma, le speranze di cura ci sono ma bisogna attendere ancora un po’ ed essere fiduciosi.
- 17/07/2018 Bambini concepiti «su misura» scegliendo colore di occhi e capelli. Modifiche genetiche accettabili?
- 03/05/2018 Creato il primo embrione in laboratorio. I prossimi esseri umani nasceranno senza genitori?
- 19/02/2018 Creato il primo embrione ibrido pecora-uomo, servirà per i trapianti d'organi
- 30/09/2017 Talassemia, la chirurgia chimica sul DNA contro l'anemia funziona